抗体に基づく次世代タンパク質製剤とバイオセンサーの開発
メンバー: 浅野竜太郎
分野: プロセス・化学工学、生物科学、生体分子科学
所属: 工学研究院生命機能科学部門
キーワード: タンパク質工学、抗体工学、二重特異性抗体、融合抗体、バイオセンサー
ウェブサイト:
研究概要

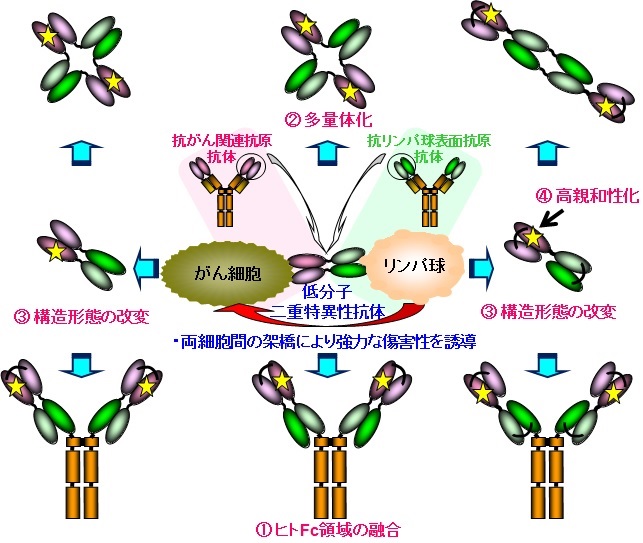
生体内の免疫に関与している抗体分子は、副作用の少ないタンパク質製剤としても利用されていますが、薬価の高さが大きな問題となっています。また従来型のIgG抗体では治療効果が限界との見方もあります。私は、一貫してがん治療を目指した組換えタンパク質、特に世界的な潮流ともなっている人工抗体医薬の開発研究に従事し、中でもがん細胞とリンパ球間の強制的な架橋により特異的な抗腫瘍効果を発揮する低分子型の二重特異性抗体の開発に注力してきました。
その過程で、がん関連抗原であるヒト上皮増殖因子受容体(EGFR)とTリンパ球上のCD3分子を標的としたEx3と名付けた分子が極めて効果的であることを見出し、さらにこのEx3の多角的な視点に基づく高機能化設計と精密機能解析を進めてきました。主に、①ヒトFc領域の融合、②多量体化、③構造形態の改変、④高親和性化の観点から高機能化を進めてきましたが、それぞれ薬効の向上が認められ、また組み合わせによりさらに機能が向上することが示されました。近年、興味深いことに同一の構造形態であっても抗体ドメインの配向性を改変するだけで活性が著しく向上することを明らかにしました。
実用化に向けては、効率的な製造プロセスの開発が残されていますが、発現微生物の検討や、精製を容易とする分子改変も視野に入れて進めていきたいと思っています。一方で、さらに魅力的な人工抗体の構造デザインや、実用的な人工抗体医薬の創製プラットフォームの開発、さらには培った組換えタンパク質の設計、および調製技術を分析・バイオセンシングを目指した生体分子の開発にも活かしていきたいと考えています。
主要論文・参考事項
- Asano R., Sone Y., Makabe K., Tsumoto K., Hayashi H., Katayose Y., Unno M., Kudo T., Kumagai I., Humanization of the Bispecific Epidermal Growth Factor Receptor x CD3 Diabody and Its Efficacy as a Potential Clinical Reagent. Clin. Cancer Res., 12(13), 4036-4042 (2006)
DOI: http://doi.org/10.1158/1078-0432.CCR-06-0059 - Asano R., Watanabe Y., Kawaguchi H., Fukazawa H., Nakanishi T., Umetsu M., Hayashi H., Katayose Y., Unno M., Kudo T., Kumagai I., Highly Effective Recombinant Format of a Humanized IgG-like Bispecific Antibody for Cancer Immunotherapy with Retargeting of Lymphocytes to Tumor Cells. J. Biol. Chem., 282(38), 27659-27665 (2007)
DOI: http://doi.org/10.1074/jbc.M704719200 - Asano R., Ikoma K., Sone Y., Kawaguchi H., Taki S., Hayashi H., Nakanishi T., Umetsu M., Katayose Y., Unno M., Kudo T., Kumagai I., Highly Enhanced Cytotoxicity of a Dimeric Bispecific Diabody, the hEx3 Tetrabody. J. Biol. Chem., 285(27), 20844-20849 (2010)
DOI: http://doi.org/10.1074/jbc.M110.120444 - Asano R., Ikoma K., Shimomura I., Taki S., Nakanishi T., Umetsu M., Kumagai I., Cytotoxic Enhancement of a Bispecific Diabody by Format Conversion to Tandem Single-chain Variable Fragment (taFv) THE CASE OF THE hEx3 DIABODY. J. Biol. Chem., 286(3), 1812-1818 (2011)
DOI: http://doi.org/10.1074/jbc.M110.172957 - Asano R., Shimomura I., Konno S., Ito A., Masakari Y., Orimo R., Taki S., Arai K., Ogata H., Okada M., Furumoto S., Onitsuka M., Omasa T., Hayashi H., Katayose Y., Unno M., Kudo T., Umetsu M., Kumagai I., Rearranging the domain order of a diabody-based IgG-like bispecific antibody enhances its antitumor activity and improves its degradation resistance and pharmacokinetics. MAbs, 6(5), 1243-1254 (2014)
DOI: http://doi.org/10.4161/mabs.29445
お問い合わせ先
東京農工大学・先端産学連携研究推進センター
urac[at]ml.tuat.ac.jp([at]を@に変換してください)
Design of next-generation biologicals and biosensors based on antibody molecules

Research members: Ryutaro ASANO PhD.
Research fields: Process/Chemical engineering, Biological Science, Biomolecular science
Departments: Department of Biotechnology and Life Science, Graduate School of Engineering
Keywords: Protein engineering, Antibody engineering, Bispecific antibody, Fusion antibody, Antibody-based biosensor
Web site:
Summary

Although antibodies have been used as molecularly targeted agents for difficult-to-treat diseases such as cancers, the high production costs associated with mammalian expression systems continue to be a drawback. In addition, the clinical efficacy of conventional IgG antibodies is limited. I have made efforts to develop recombinant small antibodies and antitumor cytokines as novel cancer therapeutic agents, and especially focused on small bispecific antibodies, which can induce specific antitumor effects by cross-linking between cancer cells and lymphocytes, and they now attract worldwide attention.
I found that a humanized small bispecific antibody (Ex3) that targets epidermal growth factor receptor (EGFR) on tumor cells and CD3 on T-lymphocytes had marked anticancer activity. Further, the function of Ex3 was enhanced by fusion with the human Fc region, multimerization, domain rearrangement, and affinity maturation; a combination of these modifications showed at least additive cytotoxic effects. Interestingly, merely rearranging the domain order of Ex3 induced substantial cytotoxic enhancements, even though the structural format remained the same.
For the development of Ex3 as a novel cancer therapeutic agent, I am working to exploit an alternative host cell system and molecular modifications to facilitate purification. I also try to develop a platform for the construction of utilized biologicals and apply these techniques in biosensing field.
Reference articles and patents
- Asano R., Sone Y., Makabe K., Tsumoto K., Hayashi H., Katayose Y., Unno M., Kudo T., Kumagai I., Humanization of the Bispecific Epidermal Growth Factor Receptor x CD3 Diabody and Its Efficacy as a Potential Clinical Reagent. Clin. Cancer Res., 12(13), 4036-4042 (2006)
DOI: http://doi.org/10.1158/1078-0432.CCR-06-0059 - Asano R., Watanabe Y., Kawaguchi H., Fukazawa H., Nakanishi T., Umetsu M., Hayashi H., Katayose Y., Unno M., Kudo T., Kumagai I., Highly Effective Recombinant Format of a Humanized IgG-like Bispecific Antibody for Cancer Immunotherapy with Retargeting of Lymphocytes to Tumor Cells. J. Biol. Chem., 282(38), 27659-27665 (2007)
DOI: http://doi.org/10.1074/jbc.M704719200 - Asano R., Ikoma K., Sone Y., Kawaguchi H., Taki S., Hayashi H., Nakanishi T., Umetsu M., Katayose Y., Unno M., Kudo T., Kumagai I., Highly Enhanced Cytotoxicity of a Dimeric Bispecific Diabody, the hEx3 Tetrabody. J. Biol. Chem., 285(27), 20844-20849 (2010)
DOI: http://doi.org/10.1074/jbc.M110.120444 - Asano R., Ikoma K., Shimomura I., Taki S., Nakanishi T., Umetsu M., Kumagai I., Cytotoxic Enhancement of a Bispecific Diabody by Format Conversion to Tandem Single-chain Variable Fragment (taFv) THE CASE OF THE hEx3 DIABODY. J. Biol. Chem., 286(3), 1812-1818 (2011)
DOI: http://doi.org/10.1074/jbc.M110.172957 - Asano R., Shimomura I., Konno S., Ito A., Masakari Y., Orimo R., Taki S., Arai K., Ogata H., Okada M., Furumoto S., Onitsuka M., Omasa T., Hayashi H., Katayose Y., Unno M., Kudo T., Umetsu M., Kumagai I., Rearranging the domain order of a diabody-based IgG-like bispecific antibody enhances its antitumor activity and improves its degradation resistance and pharmacokinetics. MAbs, 6(5), 1243-1254 (2014)
DOI: http://doi.org/10.4161/mabs.29445
Contact
University Research Administration Center (URAC),
Tokyo University of Agriculture and Technology
urac[at]ml.tuat.ac.jp
(Please replace [at] with @.)

